免疫組織化学染色(パラフィン)のポイントとコツ
このコーナーでは、定期的にバイオ・ラッドの新製品や技術情報のトピックをご紹介します。
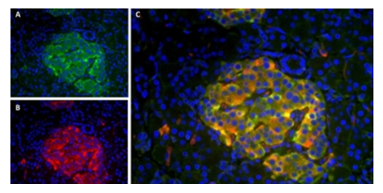
免疫組織化学染色 (Immunohistochemistry: IHC) は、酵素や蛍光色素で標識された抗体を使い、組織切片中のタンパク質を可視化するための一般的な実験手法でです。IHCは、かつては、酵素標識抗体と発色基質を用いた発色型IHCが主に行われていました。しかし近年では、複数種類のタンパク質を同時に可視化するマルチプレックス染色のニーズが高まっていることもあり、蛍光型IHCが行われることも増えています。
今回ご紹介する記事では、パラフィン包埋組織切片を対象としたIHCの概要を20ステップに分けて示し、ポイントとなるいくつかのステップについてより詳細に解説しています。
IHCの20ステップ(パラフィン包埋切片の例)
- 組織片の薄切
- スライドガラス上で切片を加熱し密着性を高める
- 脱パラフィンと切片の再水和
- (オプション)熱またはプロテアーゼによる抗原賦活化 [ Tips , (下記も参照) ]
- 洗浄
- 内在性ペルオキシダーゼ/ホスファターゼ(酵素標識抗体の場合)、およびビオチン(ビオチン/アビジン検出系の場合)のブロッキング
[ Tips , (リン酸化タンパク質を検出する場合や、アルカリホスファターゼ(,AP)標識抗体を使用する場合は、PBの代わりにトリス緩衝液(TBS)を使用)] - リン酸緩衝液(PBS)で洗浄 [ Tips ]
- ブロッキング(非特異的な結合を抑制) [ Tips ]
- 洗浄(PBSまたはTBS)
- 一次抗体との反応 [ Tips ]
- 洗浄(PBSまたはTBS) [ Tips ]
- (オプション)二次抗体との反応 [ Tips ]
- 洗浄(PBSまたはTBS)
- (オプション)増感試薬との反応 [ Tips ]
- 洗浄(PBSまたはTBS)
- DABまたは他の基質溶液との反応(酵素標識抗体の場合のみ) [ Tips ]
- ddH2Oで洗浄
- カウンターステイン [ Tips ]
- 組織切片の脱水(有機系の封入剤の場合のみ)
- カバーガラスを乗せる [ Tips ]
抗原賦活化のヒント(ステップ4)
組織を固定すると抗原のマスキングが起こり、抗体による検出ができなくなることがあります。組織固定によるこのような影響は、賦活化を行うことで部分的に回復させることができます。賦活化には、熱によるもの (HIER: Heat-Induced Epitope Retrieval) と、酵素によるもの (PIER: Proteolytic-Induced Epitope Retrieval) の2種類があります。
[抗原賦活化手法の比較]
| HIER | PIER | |
|---|---|---|
| 手法の概要 | オートクレーブ、温水槽、圧力鍋、電子レンジ、蒸し器などでサンプルを加熱 | プロナーゼ、プロテアーゼK、トリプシン、ペプシンなどの酵素でサンプルを処理 |
| 作用の原理 | エピトープの二次構造、および三次構造を復元 | エピトープを覆い隠しているペプチドを分解 |
| 使用頻度 | 最も一般的に用いられる | サンプルの形態学的な特徴を損なうことがあるため、HIERほど一般的には用いられない |
上記の他、本資料ではいくつかの主要なステップについて詳細を解説しています。パラフィン包埋組織切片のIHCの条件検討を行う際などにお役立てください。
今回の記事の関連情報
このページの情報は役に立ちましたか?
お探しの情報が見つからなかった場合やご意見など、下記までお問い合わせください。
バイオ・ラッド テックコール
life_ps_jp@bio-rad.com,
03-6404-0331(平日9:00-17:00)